PHYSIQUE, CHIMIE ET
ECUMAGE L'écumeur est un des outils indispensable au
bon fonctionnement de la méthode berlinoise. Nombre de textes ou d'articles
citent les différentes méthodes d'écumage, les dimensions
des engins, le principe de fonctionnement de l'écumeur mais bien peu
vous expliquent en détail la physique et la chimie qui se cachent derrière
cette mystérieuse boite à mousse.
I Les familles de molécules indésirables : Le bac fournit des déchets, beaucoup trop de
déchets pour le milieu clos qu'est l'aquarium qui ne peut pas détruire
seul tous ces indésirables.
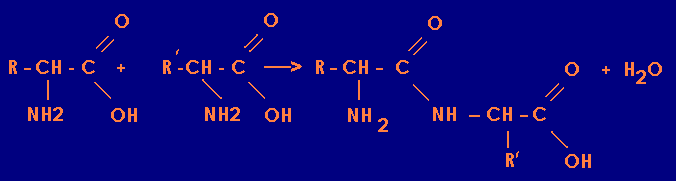
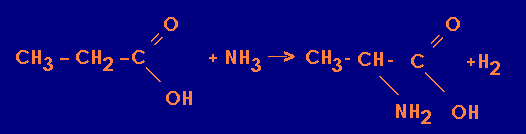 Réaction entre un acide et une amine pour donner un acide aminé Deux acides aminés s'associent entre eux pour donner un dipeptide. Plusieurs acides aminés qui s'associent donnent un polypeptide.
Lorsque le nombre d'acides aminés associés atteint plusieurs centaines, on obtient une très grosse molécule appelée macromolécule qui n'est autre qu'une protéine. Cette molécule comme beaucoup de molécules à longue chaine carbonée est colorée, ce qui donne cette couleur un peu jaune à l'eau de l'aquarium.
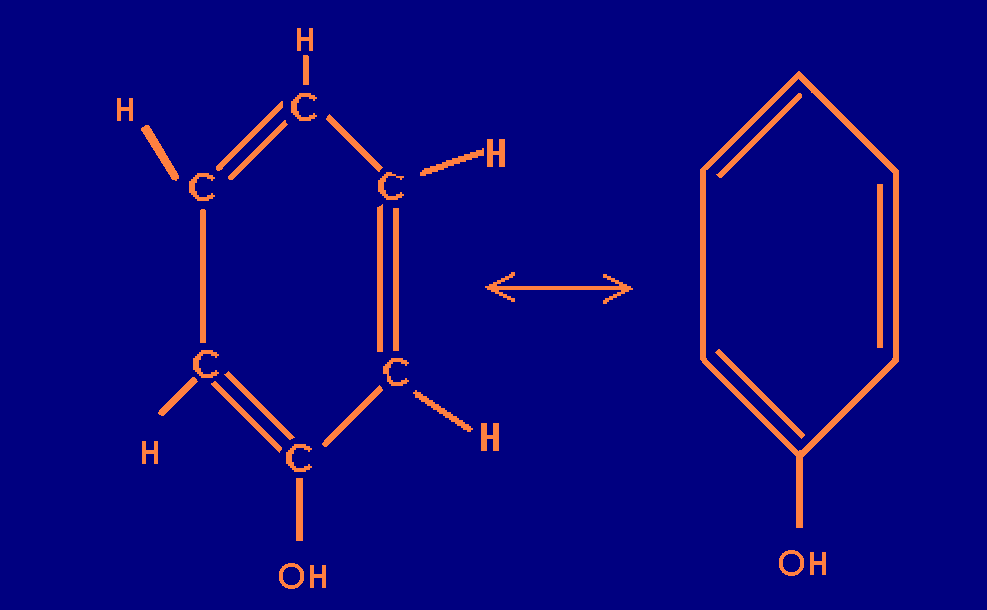
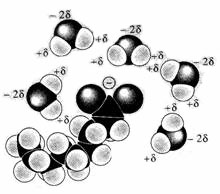
Un acide aminé, une protéine, un lipide etc… possèdent donc toujours une extrémité avec des atomes différents de l'atome de carbone (soit Azote (N), soit oxygène (O)). Or, ces atomes sont très riches en électrons libres (je rappelle qu'un atome est composé d'un noyau et d'électrons chargés négativement qui tournent autour de ce noyau). Ces électrons libres vont pouvoir établir des liaisons avec les atomes d'Hydrogène ( on les appelle liaison hydrogène et ce sont des liaisons électrostatiques, c'est à dire en rapport avec les charges apportées par chaque molécule) des molécules d'eau. On dit donc que ces molécules (acides aminés ou protéines) sont des molécules hydrophiles (qui aiment l'eau) puisqu'elles auront tendance à aller chercher l'eau pour s'y accrocher.
Mais ces molécules possèdent aussi une partie à base de carbone qui n'aime pas l'eau (hydrophobe). Pour preuve, le pétrole est constitué d'hydrocarbures dans lesquels il n'y a que des atomes de carbone et d'hydrogène, et ce pétrole n'a aucune affinité avec l'eau, il ne s'y dissout pas. Le carbone, n'étant pas riche en électrons libres, ne peut pas construire de liaisons hydrogènes avec les molécules d'eau donc il ne peut pas y avoir dissolution ou affinité entre ces queues hydrophobes et l'eau. C'est pour cela qu'on observe des marées noires. Ces molécules sont donc appelées des molécules amphiphiles puisqu'elles aiment et n'aiment pas l'eau. Elles vont donc, toute leur vie, se débrouiller pour que la tête hydrophile soit dans l'eau et que la queue hydrophobe soit hors de l'eau ou le plus loin possible de l'eau. Ces molécules sont aussi appelées des molécules tensioactives. Ces molécules vont donc être attirées par toute interface susceptible de faire en sorte que la " tête " hydrophile soit dans l'eau et la queue hydrophobe hors de l'eau. Pour récupérer ces molécules, rien de tel qu'une interface air-eau, c'est-à-dire un un contact permanent entre de l'eau et de l'air comme des bulles d'air dans l'eau. Voilà le concept de base du fonctionnement de l'écumeur.
II La tension superficielle : Pourquoi une bulle est ronde ? Voilà une question que vous ne vous êtes peut-être jamais posée? La bulle est ronde ou plutôt en forme de sphère pour diminuer la surface de contact entre les deux milieux qui constitue et entoure la bulle, l'air et l'eau. En effet, la bulle est constituée de molécules tensioactives dont une partie est dans l'eau et une partie est dans l'air, ce qui fait que ces molécules ne sont jamais satisfaites. Pour diminuer cette insatisfaction, la bulle va se mettre sous la forme d'une sphère. Quand vous écrasez dans votre main un morceau de pâte à modeler en appuyant de façon uniforme de tous les côtés vous obtenez une boule. La Terre est ronde à cause des forces de gravitation qui s'exercent vers son centre. Et bien les bulles de savon ou de molécules tensioactives, c'est la même chose. Les forces qui s'appliquent, appelées forces de tension superficielle, tendent à diminuer la surface de la pellicule d'eau qui se forme entre l'eau et l'air. Et la surface est minimale quand la forme est sphérique.
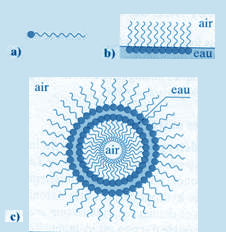
III Le principe de fonctionnement de l'écumeur : 1. La formation des bulles : Le principe de fonctionnement d'un écumeur est donc simple : on injecte de l'air d'une manière ou d'une autre dans l'eau chargée de molécules indésirables. Cet air crée une surface de contact air-eau providentielle. A la " vue " de cet air les molécules tensioactives se précipitent, trop contentes de pouvoir orienter leur queue hydrophobe vers " l'extérieur " et leur tête hydrophile vers l'eau.. On a donc formation de bulles comme le montre le schéma ci-dessous.
Sur la figure a,
on a schématisé une molécule amphiphile avec une tête
ronde hydrophile et une queue hydrophobe. Dans l'écumeur, des bulles se forment, puis sont poussées par d'autres bulles qui, à leur tour sont poussées par d'autres bulles, jusqu'à temps que cette écume sale déborde dans le godet.
Un écumeur est composé de trois parties
: La majorité du contact entre l'eau et l'air a lieu dans le corps de l'écumeur, puis la mousse chargée en molécules tensioactives monte dans le tube d'élévation pour que cette mousse puisse se séparer de l'eau " propre " et puisse sécher. Enfin, cette écume " sèche " déborde du tube d'élévation pour tomber dans le godet de récupération. 2. Le temps de contact entre l'eau et l'air : Plus les composés organiques restent en contact avec les bulles et plus elles ont de chance d'être extraites du bac. Je ne veux pas dire par là qu'une molécule " met du temps " à se placer à l'interface mais plutôt que toutes les molécules n'ont pas la même affinité pour cet interface, donc si toutes les places sur une bulle sont prises par différentes molécules il faut attendre la suivante. Lorsque vous allez à un spectacle, si toutes les places devant la scène sont prises par des gens plus rapides que vous, vous vous mettez derrière, et pour que tout le monde trouve une place il faut que la salle contienne suffisamment de places et que les portes restent suffisamment longtemps ouvertes pour que tout le monde puisse rentrer. On doit donc augmenter le temps de contact entre l'eau et l'air pour que toutes les molécules indésirables puissent être extraites. Pour augmenter ce contact, certains écumeurs injectent l'eau ou un mélange eau/air de manière tangentielle au corps de l'écumeur pour le faire tourner à l'intérieur de l'écumeur. D'autres injectent l'eau à contre courant de l'air. D'autres enfin font circuler la même eau plusieurs fois dans l'écumeur au contact de l'air. Mais je laisse à chaque fabricant ou professionnel le soin d'expliquer la meilleure durée de contact entre l'eau et l'air, ils le feront beaucoup mieux que moi. 3. La phase de séchage : Les bulles étant formées, il faut arriver
à les extraire tout en laissant dans le bac une majorité d'eau. Ce petit calcul nous montre bien tout l'intérêt qu'ont les bulles de se regrouper pour former des bulles plus grosses, minimiser donc leur surface et par là-même la tension superficielle. Remarque : Je disais donc, que l'écume se forme lorsque les bulles s'agglomèrent. Ces bulles montent poussées par d'autres bulles en laissant s'échapper l'eau prisonnière à l'intérieur de la bulle. Cette eau s'échappe de la bulle uniquement par gravité. L'attraction terrestre fait que l'eau plus "lourde" que la bulle retombe dans l'écumeur. Plus l'eau a la possibilité (et le temps) de s'échapper, plus l'écume sera sèche. C'est pour cela qu'un débit d'air trop rapide aura tendance à précipiter les bulles vers le godet de l'écumeur, ne pourra donc pas permettre à l'eau de s'évacuer assez rapidement et l'écume formée sera très humide. Le souci est que les molécules d'eau doivent pouvoir se retirer, en grande partie, sans faire éclater la bulle. Si la bulle éclate, c'est-à-dire si trop d'eau est libérée, les molécules organiques retombent, elles aussi dans la colonne. Si trop de bulles éclatent, on récupèrera beaucoup moins d'écume, donc de composés organiques mais cette écume sera beaucoup plus sèche. En résumé : Remarque : Deuxième remarque :
IV Les molécules écumées : 1. Les indésirables : Quelles sont les molécules écumées ? Je ne prendrai pas de risques en disant que cela dépend
des écumeurs. On est tous d'accord pour constater que des écumeurs
de types différents ou de marques différentes ne vont pas écumer
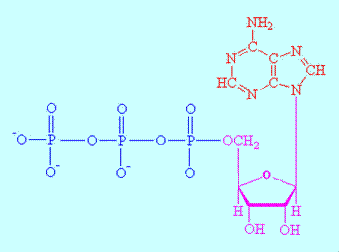
la même chose. Les phosphates sont de deux natures : Commençons par les phosphates inorganiques de formule PO43- qui ne sont en aucun cas tensioactifs puisqu'ils ne possèdent pas de partie hydrophobe. Ils n'ont donc aucun intérêt à se trouver à l'interface air/eau et ne sont pas écumés. Les phosphates organiques sont présents directement dans les êtres vivants, comme par exemple dans les molécules d'ADP ou d'ATP. Les phosphates organiques constituent des "réserves d'énergie": adénosines mono-, di- et triphosphate (AMP, ADP et ATP), créatine, phosphate de l'acide glycérique, etc. Ces corps interviennent dans les cycles respiratoires et dans l'activité musculaire. L'ATP, par exemple, est une molécule organique composée d'adénine, de ribose (un sucre) et de trois molécules d'acide phosphorique. L'ATP est formé par fixation, grâce à l'énergie tirée de la respiration cellulaire (ou de la photosynthèse), d'une molécule d'acide phosphorique sur une molécule d'acide adénosine-diphosphorique (ADP). Inversement, il fournit, par libération d'une molécule d'acide phosphorique, l'énergie nécessaire aux réactions endergoniques de l'organisme.
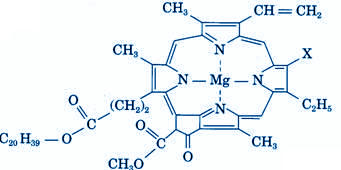
Autre exemple de phosphate organique, cette molécule glycérophospholipide qui fait partie de la famille des lipides. Cette molécule est hydrophobe par ses deux chaines carbonées et hydrophile par son groupe phosphate. Les glycérophospholipides constituent les membranes biologiques des êtres vivants. Ce qui sous entend que tous les micro-organismes ou tous les animaux unicellulaires comme le plancton sont extraits par l'écumeur. Restent les nitrates, qui, de toute façon, sont " enlevés " par les pierres vivantes mais, ne sont pas retirés par l'écumeur puisque ne présentent pas de caractère hydrophobe. 2. Les indispensables : Mais l'écumeur peut retirer aussi des oligo-éléments
que l'on aimerait garder dans le bac.
V Facteurs influençant l'écumage
Les premiers facteurs influençant l'écumage
sont, la taille des bulles, la durée de contact entre l'eau et l'air,
la quantité d'eau et d'air injectés. · 1 bulle de 1 m de rayon, possède une
surface d'à peu près de 12 m2 et un volume de 4 m3. On constate donc qu'un même volume d'air injecté
peut créer 10 fois plus d'interface air/eau s'il est injecté
sous forme de bulles 10 fois plus petites. Ce résultat est éloquent
et permet de comprendre pourquoi il faut diffuser de très fines bulles. 2. Circulation d'eau dans le bac : En ce qui concerne la circulation d'eau dans le bac, je peux préciser, même si cela peut paraître évident qu'un maximum d'eau de l'aquarium doit circuler au voisinage de l'écumeur. Il est donc, à mon sens, très important d'avoir un brassage important dans le bac, avec une sortie d'eau et une remontée d'eau dans des coins opposés de la cuve et une circulation d'eau importante dans la cuve technique. Le meilleur rendement doit être obtenu avec une " circulation forcée " de l'eau dans la cuve technique (donc installation de chicanes) pour ne pas traiter la même eau plusieurs fois. Il est également très important d'avoir un débordement dans le bac principal puisqu'on a vu plus haut que les molécules tensioactives cherchent l'interface eau-air ; donc en recueillant dans la cuve technique l'eau de surface, on écume d'autant mieux les corps gras.
3. Ozone et écumage : L'ozone de formule O3 est un oxydant très puissant, que l'on utilise en particulier dans la chimie industrielle. Cette molécule est présente dans l'atmosphère terrestre à deux " niveaux " : - En haute atmosphère, sous forme de couche,
et joue le rôle de filtre anti-UV contre les UV les plus agressifs qui
nous viennent du Soleil. L'ozone se transforme selon la réaction suivante
: L'ozone oxyde les molécules en ajoutant un atome d'oxygène donc, de ce fait, les rend plus hydrophiles. L'ozone "coupe" en petits morceaux certaines macromolécules comme les protéines, mais est-ce que cela change la quantité de molécules organiques extraites par l'écumeur ? Les articles traitant de ce sujet sont assez flous et pas toujours en accord. Il me semble donc qu'il faut être prudent sur la question tant que l'on n'aura pas fait des études détaillées et comparatives. Conclusion : voilà encore une fois de longs et beaux discours théoriques qui nous laissent tous un peu rêveur… et un peu inquiet surtout. C'est vrai que, quand on creuse un peu, on s'aperçoit que la physique et la chimie sont présents partout en aquariophilie même dans des phénomènes aussi simples en apparence que la formation et l'éclatement d'une bulle. Mais ne pas trop s'inquiéter il faut, chacun ayant ses réglages et ses petits "trucs" pour que toute notre population se trouve le plus à l'aise possible. La pensée du jour pour terminer (qui revient
souvent en aquariophilie) : en théorie, voilà comment cela se
passe!
|